新型视网膜成像技术可直接测量活体视杆细胞功能
原创 青白视角 青白视角
2026年1月10日 15:51 美国 标题已修改
2026 年 1 月 7 日,由新加坡南洋理工大学、美国华盛顿大学医学院、新加坡国家眼科中心/新加坡眼科研究所及杜克-新加坡国立大学医学院等机构联合组成的研究团队,在《Light: Science & Applications》(Nature旗下Top期刊,中科院1区,IF:23.4)在线发表了题为《Optoretinography reveals rapid rod photoreceptor movement upon rhodopsin activation》(《光视网膜成像揭示视紫红质激活时视杆光感受器的快速运动》)的研究论文。

本研究通讯作者为新加坡南洋理工大学的Tong Ling(凌曈)教授和美国华盛顿大学医学院的Ramkumar Sabesan教授。这项研究汇聚了来自多机构的生物医学工程师、物理学家和临床科学家,包括新加坡眼科研究所及杜克 - 新加坡国立大学Leopold Schmetterer教授团队和Veluchamy Amutha Barathi副教授团队 —— 他们为研究提供了视网膜成像和啮齿动物模型方面的关键专业支持。团队成员涵盖工程学、物理学、生物学、眼科学等多个领域,通过光学成像技术、信号处理算法与视网膜生理机制研究的深度交叉,突破了传统研究瓶颈。
视杆细胞负责暗视觉,约占人类视网膜感光细胞的 95%,也是年龄相关性黄斑变性(AMD)、视网膜色素变性(RP)等致盲性视网膜疾病中最先受损的细胞之一。传统视杆细胞功能检测存在显著局限:在体技术灵敏度、特异性和细胞分辨率不足,离体方法具有侵入性无法应用于活体,且诊断过程耗时,给患者带来负担。此前,相关研究主要依赖电生理技术和生化分析,虽能提供部分价值信息,却无法捕捉视紫红质所在的孤立盘膜内的电活动,也难以精准捕获视杆细胞激活过程中细微的物理运动 —— 其空间与时间尺度一直是研究难点。
针对这一痛点,研究创新性采用超高分辨率点扫描 OCT 系统结合无监督学习算法,以及自适应光学线扫描 OCT 技术,实现了视杆细胞的无创在体成像。视杆细胞内的光敏蛋白 —— 视紫红质在视觉信号转导级联中发挥着至关重要的作用——它将光子吸收转化为与大脑沟通的电信号。该研究核心发现显示,当视紫红质吸收光子(光激活)时:视杆细胞外节会在毫秒内发生微小收缩:啮齿动物收缩幅度可达 200 纳米(这是天然生物细胞中已观测到的最大机电变形,远超皮质神经元动作电位期间约 1 纳米的典型变形),人类收缩幅度饱和时约 100 纳米。这种结构形变在光照后几毫秒内即可测量,凸显了视杆细胞机械行为比先前假设的更为快速和动态。这些发现不仅证实了视杆细胞除了生化信号传导之外还具有响应能力,而且还揭示了光感受器功能的一个潜在新维度——机械调节。
在技术层面,此次研究所用的光视网膜成像(ORG)技术,是基于光学相干断层扫描的无创高分辨率成像方法,专门用于检测光诱发的光感受器活动。尤其在人眼试验中,该技术整合自适应光学(可区分视杆与视锥细胞)和干涉测量(能精准测量微小距离与表面不规则性)两大关键技术,形成了全新的高灵敏度检测方式:无需染料、电极或侵入性探针,即可在细胞层面可视化视网膜功能,成功捕获到此前难以企及的视杆细胞电信号相关动态。其超高灵敏度可有效区分光转导引起的运动与血流等其他视网膜动力学因素导致的运动,这种特异性为明确视紫红质激活与视杆细胞机械变化的关联提供了关键支撑。
机制层面,该收缩现象由早期感受器电位引发的机电耦合效应导致,与电压依赖性膜张力模型高度吻合 —— 即便将一次强刺激拆分为一系列较弱的连续刺激,测得的累计收缩幅度仍与模型预测结果一致,充分印证了模型可靠性。而视杆细胞的机械 “收缩” ,正是视紫红质激活所产生的电活动引发机电作用力的直接体现。
值得关注的是,视杆感光细胞运动速度极快(仅需几毫秒),引发了对其生物学功能的诸多探索:有观点认为,这些运动可能通过调节生化环境或影响信号传播速度来增强感光细胞的性能。也有观点提出,它们可能具有保护作用,最大限度地减少光子吸收造成的分子损伤,这些潜在作用仍需未来研究进一步阐明。
随着全球人口老龄化和视网膜疾病对生活质量的影响日益加剧,阐明微观尺度视网膜功能的创新技术变得至关重要。而本研究提出的技术,能通过客观、高分辨率的功能评估,更早捕捉到视杆细胞功能异常(该指标早于传统检测中的视觉灵敏度丧失),为视网膜退行性疾病的早期诊断、疾病进展评估及治疗反应监测提供了全新路径,有望推动眼科疾病个性化治疗的发展。
团队与专家评价
研究负责人、南洋理工大学Tong Ling(凌曈)教授表示:“眼睛夜视细胞的‘颤动’,就如同视觉的点火火花。我们早就知道这些细胞吸收光线时会产生电信号,但此前从未有人在人类或啮齿动物的活体眼睛中,观察到这些细胞伴随的机械收缩现象。这一发现揭示了视杆光感受器探测光线并向大脑传递视觉信息过程中的关键基础步骤。这些细胞约占人类视网膜所有感光细胞的 95%。”
共同通讯作者、华盛顿大学医学院视觉科学家Ramkumar Sabesan教授表示:“这是我们首次在活体眼睛的视杆细胞中观察到这一现象。视杆细胞功能障碍是多种视网膜疾病(包括年龄相关性黄斑变性和视网膜色素变性)最早出现的症状之一。能够直接监测视杆细胞对光的响应,为我们提供了一种强大的工具,可比任何传统诊断设备更早、更灵敏地检测疾病并追踪治疗效果。”
德国海德堡大学眼科系主任、眼科医生兼临床科学家Jost Jonas教授进行了独立评论:“光视网膜成像作为一项全新技术,在临床和科学领域都极具吸引力和应用前景 —— 它首次实现了无创可视化活体人眼细胞结构的纳米级运动,这既适用于作为感光细胞的视杆细胞,也适用于视网膜中的其他细胞。”“因此,它可能为深入理解视网膜细胞的工作机制及其与邻近细胞的相互关系开辟新途径,同时在临床上有望更细致、甚至更早地诊断视网膜疾病,尤其是那些主要影响感光细胞的病症。”
相关图表:

图1:采用相位分辨 OCT 记录强漂白(bleaching)刺激(5 毫秒,波长 505 纳米,34.0% 漂白水平)下视网膜外层的多层动态变化。

图4:闪光间隔 15 秒的 5 次闪光诱发的视杆细胞外节(OS)响应
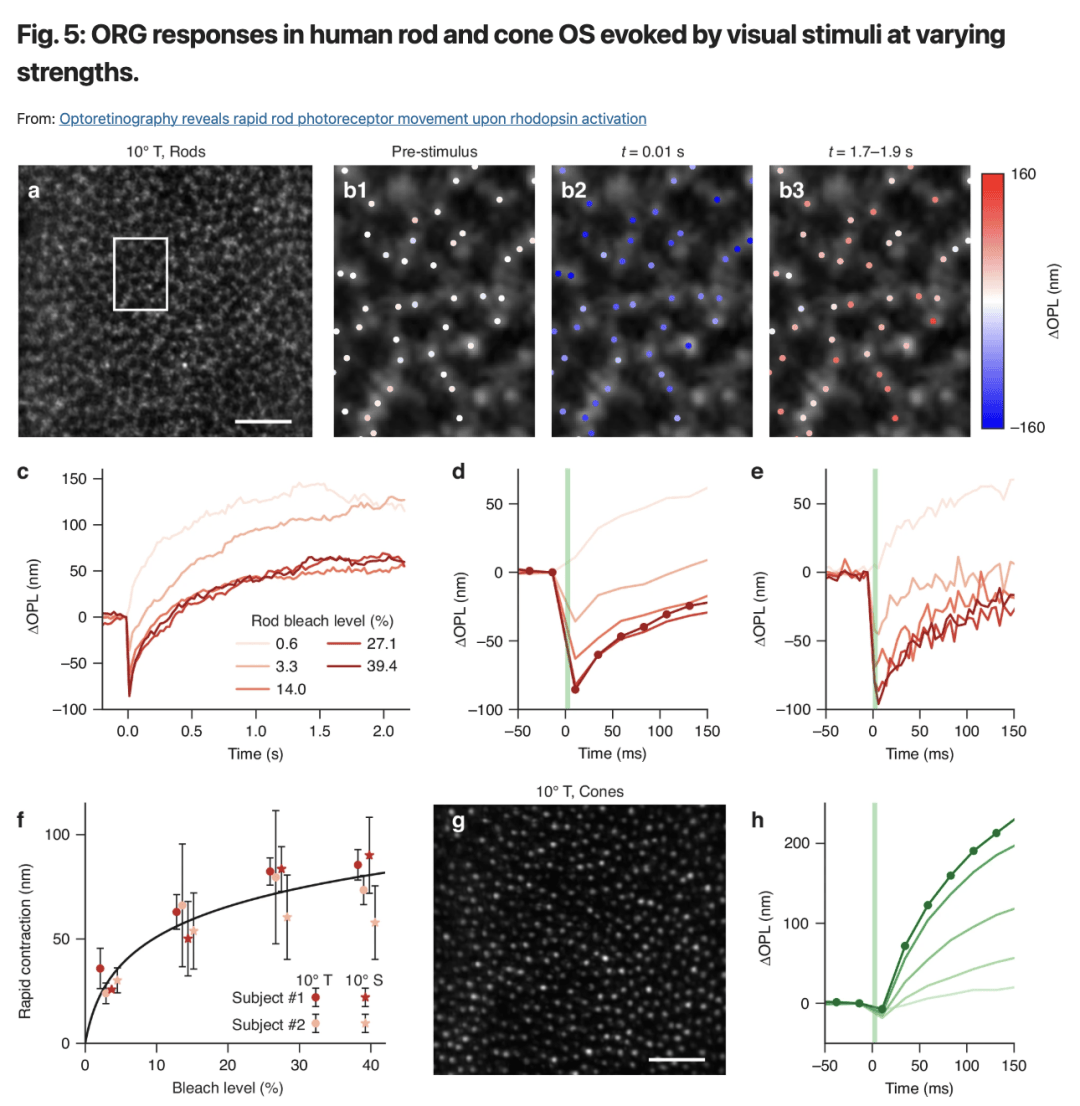
图5:不同强度视觉刺激下人类视杆和视锥细胞外节的光视网膜成像(ORG)响应
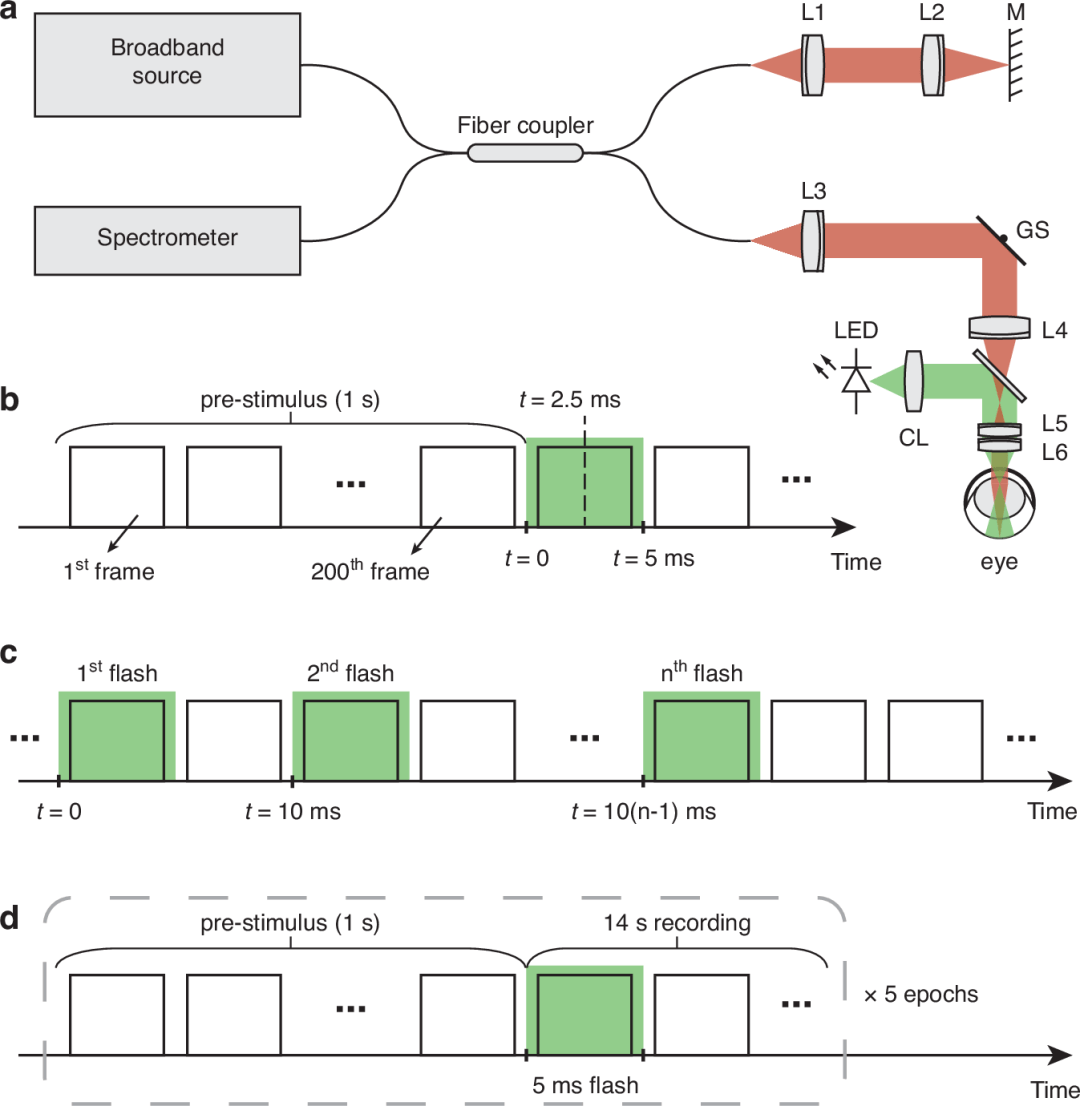
图6:数据采集与视觉刺激的系统装置及时序图
本文相关文献:
Li, H., Weiss, C.E., Pandiyan, V.P. et al. Optoretinography reveals rapid rod photoreceptor movement upon rhodopsin activation. Light Sci Appl 15, 58 (2026). https://doi.org/10.1038/s41377-025-02149-6
