柏林工业大学——革新心血管疾病诊断:基于纳米分子印迹和便携式SPR技术的即时护理传感器
文章导读
在现代社会,心血管疾病 (CVD) 是导致死亡的主要原因之一,其诊断的及时性和准确性对治疗效果至关重要。心血管疾病的早期诊断对于提高治疗效果和降低死亡率非常关键。传统的检测方法往往耗时较长,并需要专业的设备和技术人员。因此,开发快速、灵敏、特异且便携的检测技术是当务之急。本篇由柏林工业大学Zeynep Altintas团队撰写并发表于 Biosensors 期刊的文章开发了一项创新技术,为心血管疾病的快速诊断带来了希望,这项技术基于表面等离子共振 (SPR) 传感器,通过使用表位印迹的分子受体来检测心脏肌钙蛋白I (cTnI),这是一种在心肌梗死时其在血液中的含量会急剧上升的生物标志物。该研究通过精确的表面覆盖和纳米分子印迹聚合物 (nanoMIPs) 的尺寸优化,实现了对cTnI的高灵敏度检测,具有重要临床意义。
研究过程和结果
研究人员首先使用11-巯基十一酸 (MUDA) 等化合物和方法制备了能够固定在SPR传感器芯片上的nanoMIPs。通过动态光散射 (DLS) 和荧光显微镜技术对nanoMIPs的表面覆盖率和大小进行了表征。在制造过程中,使用原子力显微镜 (AFM)、电化学阻抗谱 (EIS)、方波伏安法 (SWV) 和循环伏安法 (CV) 技术验证了每一步传感器制造的成功实施。这些技术不仅确认了nanoMIPs的成功固定,还确保了传感器的高灵敏度和特异性。
新型SPR传感器针对cTnI肽模板进行了初步建立,允许在100—1000 nM的浓度范围内检测肽,相关系数 (R2) 为0.96,检测限 (LOD) 为76.47 nM。进一步优化的检测条件允许在0.78—50 ng/mL的宽浓度范围内检测cTnI生物标志物,具有高重复性 (R2=0.91) 和灵敏度 (LOD:0.52 ng/mL)。传感器结果受到三种结合等温模型的评估,其中nanoMIP-cTnI相互作用遵循Langmuir结合等温模型,解离常数为2.99 × 10−11 M,表明cTnI生物标志物与表位印迹合成受体之间有极强的亲和力。通过使用非特异性肽模板制备的对照nanoMIP进行选择性研究,以及对非特异性分子 (例如葡萄糖、p53蛋白、转铁蛋白和牛血清白蛋白) 进行交叉反应性测试,证实了nanoMIP-SPR传感器对目标生物标志物具有高特异性。
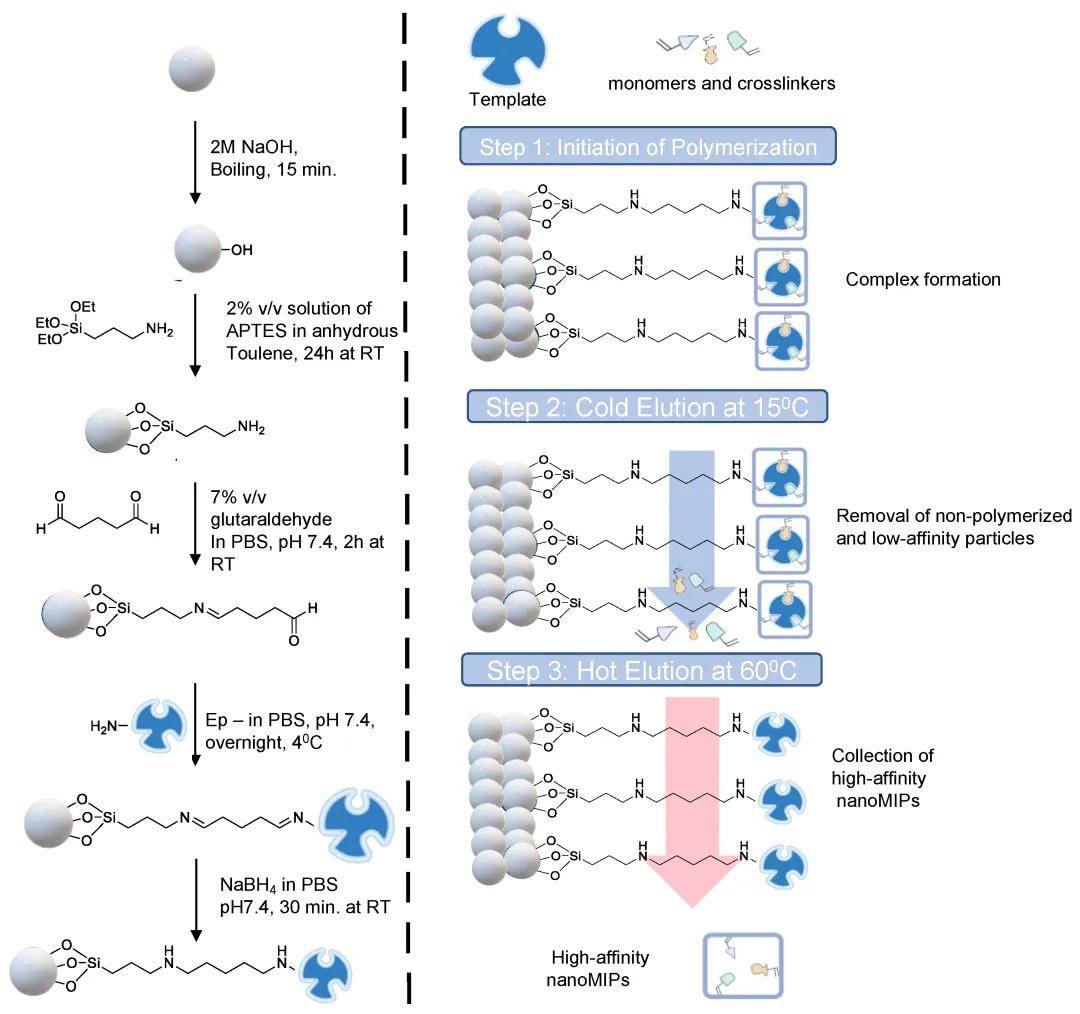
- 图1. 表位模板固定在玻璃珠上作为固体载体 (左) 和三步固相合成 (右) 的示意图。
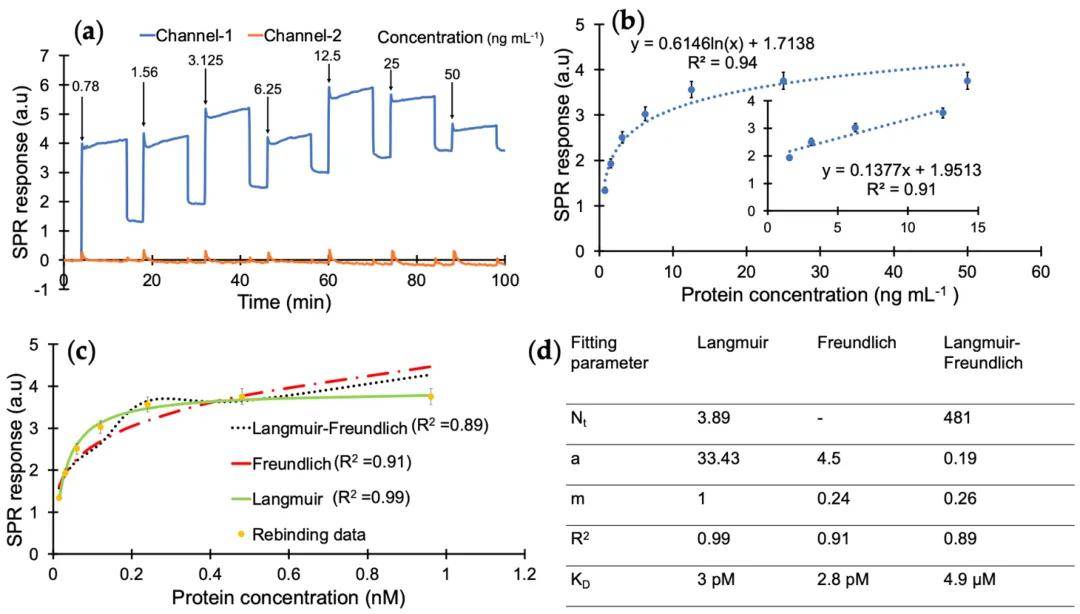
- 图2. (a) 累积cTnI检测的实时SPR传感器图。(b) 浓度依赖性蛋白结合,在线性范围内相关系数为0.94,R2值为0.911.56—12.5 ng mL-1。(c) 纳米omip与cTnI相互作用的结合等温线拟合。(d) 从Langmuir、Freundlich和Langmuir-Freundlich模型中获得的结合等热拟合参数。
文章总结
本研究成功开发了一种基于表位印迹的便携式SPR传感器,用于快速、灵敏地检测心肌梗死生物标志物cTnI。该传感器具有操作简便、成本效益高、无需标记和高亲和力等优点,为心肌梗死的早期诊断和护理点检测提供了一种有力的工具。这项研究的成果不仅对心血管疾病的诊断具有重要的临床意义,而且对生物传感器技术的发展也具有推动作用。便携式SPR传感器的开发,有望在未来的医疗检测领域中发挥更大的作用,特别是在远程医疗和个人健康监测方面。未来,研究团队将进一步优化传感器的性能,提高检测的准确性和稳定性,并探索其在其他疾病标志物检测中的应用潜力。同时,也将致力于传感器的商业化进程,使其更广泛地应用于临床实践。
原文出自 Biosensors 期刊
houdhary, S.; Altintas, Z. Development of a Point-of-Care SPR Sensor for the Diagnosis of Acute Myocardial Infarction. Biosensors 2023, 13, 229. https://doi.org/10.3390/bios13020229
Biosensors 期刊介绍
期刊主要发表生物传感器及其技术和应用方面的研究论文。内容涵盖DNA芯片、微流体装置、纳米生物传感器及其应用、生物传感器制造、生物传感器材料、芯片实验室技术和生物传感器在生物医药、食品质量与安全等领域的应用。
2024 Impact Factor: 5.6
2024 CiteScore: 9.8
